Las soluciones pueden generar cátodos o precipitados con zinc. La electrodeposición es el método convencional. La precipitación con zinc es usada extensamente directamente en la solución rica. El zinc puede usarse para precipitar oro de una solución de la elución del carbón cargado. Varias ventajas lejos el uso de zinc sobre electrodeposición pueden considerarse. Estos incluyen: la inversión de capital es menor; remoción eficiente de metales preciosos de la solución; y menores costos operativos.
Electrodeposición
La electrodeposición remueve los metales preciosos de la solución obtenida del proceso de elución por el paso de corriente a través de una celda de electrodeposición. El cátodo, el ánodo, y un electrólito son colocados en un recipiente resistente a la corrosión. Un suministro de energía esta conectado al ánodo y el cátodo. Como la corriente atraviesa la celda, el metal es depositado en el cátodo. El compartimiento de la celda es de un flujo lineal o radial. Como el metal es removido del electrólito, una solución fresca ingresa la celda reemplaza la solución agotada a través de los puntos de circulación considerados.
El cátodo se hace de un conductor con una apropiada área superficial. La superficie extendida está obligada a minimizar la densidad de corriente (corriente total respecto del área superficial del cátodo). Esto ayuda a la transferencia del metal a la superficie del cátodo. Como la concentración de los metales decrece, la eficiencia de la celda también disminuye. Esto es demostrado por la formación de hidrógeno en el cátodo con densidades de corriente altas.
El cátodo puede ser de varios diseños. Los requisitos principales incluyen: 1) alta área superficial; 2) una gran área para la deposición de metales y el flujo de electrólito; 3) conductividad alta; 4) buena fuerza resistencia mecánica. Una celda típica usa un marco plástico con una lana de acero empacando de dos a cuatro pulgadas de espesor. El área de la sección transversal del marco es determinada por el flujo de solución a través de la celda de electrodeposición. En una celda rectangular con flujo lineal, los cátodos son suspendidos abajo del eje central de la celda alternándose con los ánodos. En la celda original Zadra con flujo radial, la lana de acero estaba holgadamente envuelta alrededor de un carrete de acero inoxidable con el ánodo acomodado concéntricamente alrededor del cátodo. Ciertas celdas pueden usar una cama fluidizada o compactada de partículas como el cátodo.
El ánodo también debe ser una superficie conductiva, un metal típicamente plano o curvado. La superficie puede ser una plancha agujereada, una lámina lisa, o una malla; Aunque también puede ser un conductor extendido parecido al cátodo. El ánodo debe ser resistente a la corrosión bajo las condiciones altamente oxidantes en el contacto con el electrólito. El acero inoxidable es el material típico de construcción, aunque el carbón o el titanio también puede ser usado. En ciertas celdas, las paredes de la celda pueden servir del ánodo. En una celda rectangular, el ánodo, una plancha agujereado o una malla, está suspendida en la celda alternándose con los cátodos. La energía eléctrica es transmitida a los electrodos por barras hacia cada lado de la celda. En la celda Zadra, el ánodo es una malla de acero inoxidable cilíndrica acomodada concéntricamente fuera del cátodo. Con camas fluidizadas, el ánodo es a menudo la pared externa de la celda.
El electrólito a una temperatura adecuada, ingresa a la celda de electrodeposición con una concentración alta de metales preciosos. La solución obtenida de la elución puede ser circulada a través de una sola celda o una serie de celdas. El cobre, el mercurio, la plata, y el oro contento de la solución son ingresados en el cátodo como metales a medida que la solución fluye a través de la celda. La solución ingresa con una concentración de metales preciosos que varía de 2,000 ppm a 50 ppm. Como el metal precioso es extraído del carbón, el grado de solución decrece. Una vez que el carbón es eluido hasta un nivel residual de oro de cinco oz/t, el carbón es considerado sin carga de metales. Mientras más baja sea la concentración de metal en el electrólito, la remoción de metal es más difícil. La temperatura de electrólito no es crítica con tal de que la solución sea enfriada debajo del punto de ebullición antes de ingresar a la celda de electrodeposición. Cuando se usa material plástico, la solución puede requerir un posterior enfriamiento a cerca de 140 oF.
La operación de la celda depende del flujo de circulación, el voltaje, y la conductividad de solución. La velocidad de solución en la celda determina las características de la transferencia de metal en la celda. Las tasas superiores de circulación dentro de la celda mejoran la transferencia de la masa y da mejores depósitos de metal en el cátodo. La conductividad del electrólito, distancia entre el ánodo y el cátodo, y la corriente específica determinan voltaje de la celda.
La energía requerida para la electrodeposición está determinada por lo corriente y el voltaje. Aproximadamente 2.5 voltios son aplicados entre el ánodo y el cátodo de una celda. La eficiencia se acerca al 100 por ciento en 2,000 ppm de oro y de 0 por ciento en 1 ppm de oro. El capital de inversión, y el suministro de energía a menudo pueden ser significativos. Los costos operativos se relacionan a la labor. Los electrodos deben ser soportados con contacto conductivo para el suministro de energía eléctrica.
Cuando suficiente metal ha sido ingresado en el cátodo, el cátodo es una masa de lana de acero barrosa, y es removido, enjuagado y secado. El lodo del fondo de la celda es también removido periódicamente para el tratamiento para recobrar el metal precioso.
Diseños de Celdas de Electrodeposición
Los diseños de varias celdas de electrodeposición han sido desarrollados durante varios años para mejorar la eficiencia de electrodeposición de metales preciosos. Estos diseños incluyeron a la celda Cilíndrica Zadra, la celda A.A. R.L. la celda de diafragma, la celda Micron, y la celda de fibra de carbón HSA (de alta área superficial). Sin embargo, hoy un diseño es casi universalmente seleccionado para operaciones nuevas de cualquier tamaño. Este es un tanque rectangular que acomodan pares de cátodos y ánodos múltiples suspendidos verticalmente de barras de distribución de energía eléctrica.
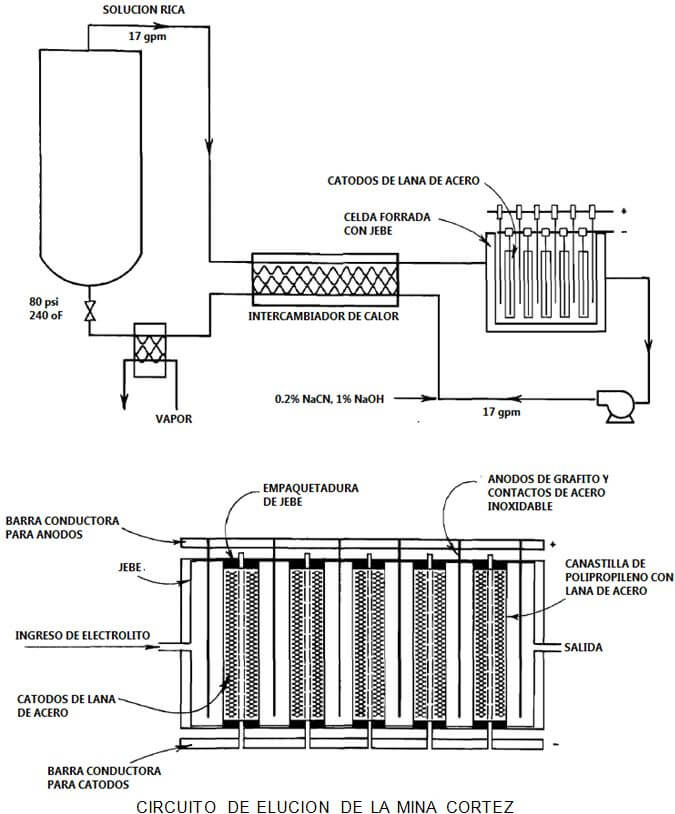
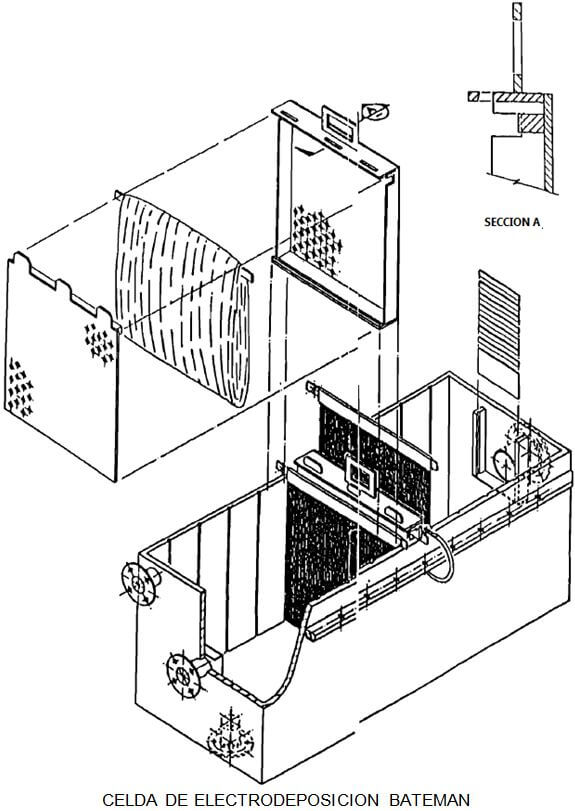
La siguiente figura muestra el arreglo de elución de la mina de oro de Cortez, y otra figura muestra la celda Bateman.
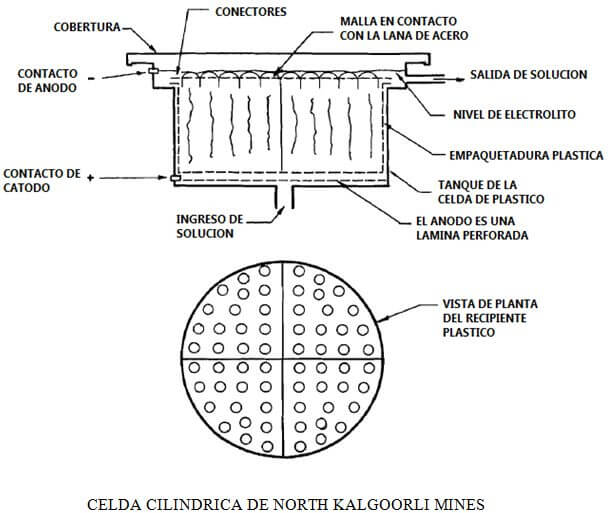
El ánodo de la celda cilíndrica Zadra es una malla de acero inoxidable cilíndrica situada fuera del cátodo. Ambos, el envase del cátodo y el ánodo son situado interiormente de modo que la celda consiste en un tanque cilíndrico. La solución concentrada fluye a través del tubo central y luego fluye hacia arriba y hacia afuera a través de la lana de acero.
Las desventajas de la celda Zadra son la distribución no homogénea de la solución, el espaciamiento de los electrodos, el cátodo de lana de acero es grueso y origina una caída de potencial, cada celda contiene solo un par cátodo – ánodo, y las celdas son un solo cuerpo.